-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaTrombózy v gynekologii a porodnictví
Datum publikace: 7. 12. 2015
ÚVOD
V zemích Evropské unie je jedno z 10 úmrtí spojeno s trombembolickou komplikací. Jedná se o třetí nejčastější příčinu kardiovaskulárního úmrtí po infarktu myokardu a ischemické cévní mozkové příhodě.
Nejčastější prezentace žilní trombózy je hluboká žilní trombóza (deep venous thromboembolism - DVT) dolních končetin a plicní embolie. Příčiny žilní trombózy mohou být rozděleny do dvou skupin: dědičné a získané, a jsou často mnohočetné u daného pacienta. Dědičné trombofílie jsou podmíněny geneticky, projevují se v mladším věku a často recidivují. Trombózy v gynekologii a porodnictví mají svoje specifika, která budou zmíněna dále v textu.
Rizikové faktory (příčiny) vzniku žilní trombózy
Dědičné trombofilie

Získané poruchy
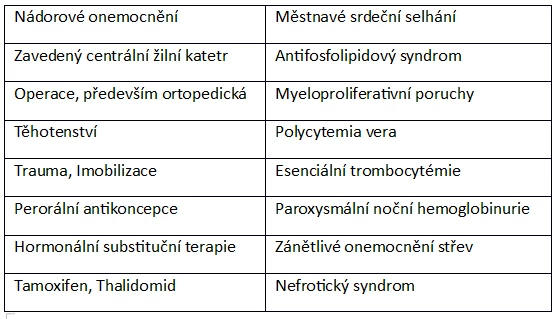
Hlavní teorií dokreslující mechanizmus vzniku žilního tromboembolizmu (venous thromboembolism - VTE) je tzv. Virchowova trias, pro kterou jsou charakteristické [i,ii]:
- Změny v průtoku krve (tj. městnání)
- Cévní endoteliální poranění
- Změny v složení krve (tj. vrozené nebo získané hyperkoagulační stavy)
Rizikový faktor pro vznik trombózy může být identifikován více jak u 80 procent pacientů s žilní trombózou. Často bývá přítomno více rizikových faktorů u jednoho pacienta. Například až padesát procent trombotických příhod u pacientů s dědičnou trombofilií je spojených s přítomností získaného rizikového faktoru (např. chirurgický zákrok, prodloužený klid na lůžku, těhotenství, perorální antikoncepce). Někteří pacienti mají více než jednu formu zděděné trombofílie nebo více než jednu formu získané trombofilie a jsou tak v ještě větším riziku rozvoje trombózy.
Povrchová žilní trombóza
Povrchová žilní trombóza (superficial venous thrombosis - SVT) je méně závažné onemocnění než hluboká žilní trombóza. Vyskytuje se u zděděných i získaných trombofilních stavů, a může vyústit v hlubokou žilní trombózu a/nebo plicní embolii [iii, iv, v, vi]. U 63 pacientů, kde byla ultrazvukem potvrzena SVT dolních končetin bez dalších rizikových faktorů bylo pozorováno [vii]:
- Dvacet pacientů (32 procent) vyvinulo DVT do 4 let
- Patnáct pacientů (24 procent) mělo opakované epizody SVT.
Dědičné trombofilie
Jako dědičné trombofilie jsou označovány stavy s genetickou tendencí k tromboembolické nemoci. Mezi nejčastější příčiny dědičného (primární) hyperkoagulačního stavu jsou mutace faktoru V Leiden a mutace protrombinu, které dohromady představují 50 až 60 procent případů vzniku DVT. Defekty v proteinu S, proteinu C, a antitrombinu (dříve známý jako antitrombinu III) představují většinu ostatních případů, zatímco nejvzácnější příčinou je dysfibrinogenémie [viii, ix,x, xi].
Hluboká žilní trombóza
Prevalence dědičných trombofílií u pacientů s hlubokou žilní trombózou se pohybuje v rozmezí 24 až 37 procent.
Pravděpodobnost vzniku trombózy v rodinách s prodělanou tromboembolickou nemocí (TEN) ve srovnání s těmi bez TEN byla 8,5 krát vyšší pro nositele deficitu proteinu S, dále 8,1 krát vyšší pro nositele deficitu antitrombinu, dále 7,3krát pro nedostatek proteinu C, a 2,2krát pro mutaci faktoru V Leiden. Riziko u postižených žen bylo v průběhu těhotenství a užívání perorální antikoncepce rovněž vyšší.
U ostatních dědičných trombofílií zůstává nejasné, zda některé z těchto onemocnění jsou ve skutečnosti spojeny se zvýšeným rizikem žilní trombózy.
Dysfibrinogenémie - pacienti s dysfibrinogenémií mají strukturální vady, které způsobují změny v konverzi fibrinogenu na fibrin. Frekvence, s jakou nedostatečnost faktoru XII vede k trombóze, je nejistá.
Získané rizikové faktory nebo predispozice k trombóze: patří mezi ně předchozí trombotická příhoda, poslední velký chirurgický zákrok, přítomnost centrálního žilního katetru, trauma, imobilizace, malignita, těhotenství, užívání antikoncepčních pilulek nebo heparinu, myeloproliferativní onemocnění, antifosfolipidový syndrom (APS), a celá řada dalších nemocí.
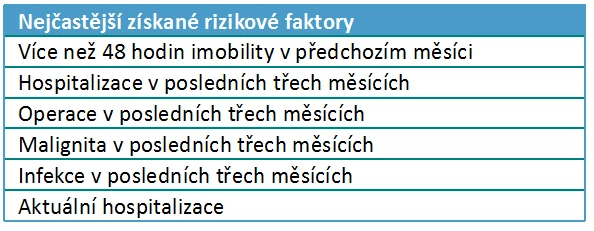
Kombinované získané a vrozené rizikové faktory
Jak bylo uvedeno výše, u pacientů s VTE může být více dědičných vad nebo více získaných rizikových faktorů pro VTE. Kromě toho mohou být rovněž kombinace obou, tedy dědičných i získaných trombofilních vad.
Předchozí tromboembolizmus
Předcházející trombotické epizody jsou významným rizikovým faktorem pro recidivující VTE. V ambulantní prospektivní studii bylo riziko recidivy po akutní epizodě žilní trombózy 18, 25, a 30 procent ve dvou, pěti, a osmi letech [xii]. Relativní riziko (RR) pro recidivu VTE je 7,9[xiii].
Přítomnost nebo nepřítomnost rizikových faktorů (např. těhotenství, chirurgický zákrok) se stává důležitou informací v terapeutickém přístupu k pacientům s první, nebo opakující se epizodou VTE.
Malignita
Pacienti s rakovinou mají často hyperkoagulační stav vzhledem k tvorbě látek s prokoagulační aktivitou (např. tkáňový faktor). Klinická žilní tromboembolie se vyskytuje u přibližně 5 procent těchto pacientů a je častou příčinou vážných klinických důsledků, včetně významného krvácení a smrti, a to zejména u starších pacientů, jakož i u malignit spojených s pokročilým onemocněním v době diagnózy (např. rakovina pankreatu) [xiv, xv, xvi]. Riziko VTE u těchto pacientů se zdá být největší během počáteční hospitalizace, počátkem chemoterapie a v době progrese onemocnění [64].
Riziko trombózy může být u pacientů s malignitou a zavedeným centrálním žilním katetrem vysoké a to až 12 procent [65-68].
Přibližně 20 procent pacientů se symptomatickou hlubokou žilní trombózou mají známou aktivní malignitu [45,69]. V retrospektivní studii více než 63000 pacientů přijatých do dánských nepsychiatrických nemocnic z let 1977 až 1992 pro diagnózu VTE, 18 procent mělo diagnózu rakoviny před tromboembolickou příhodou [70].
Většina malignit spojených s tromboembolickou příhodou je klinicky evidentní a byly diagnostikovány ještě před vznikem DVT. V dánské studii, bylo známo 78 procent případů s anamnézou rakoviny [70].
Největší riziko vzniku VTE je u těchto typů karcinomu:
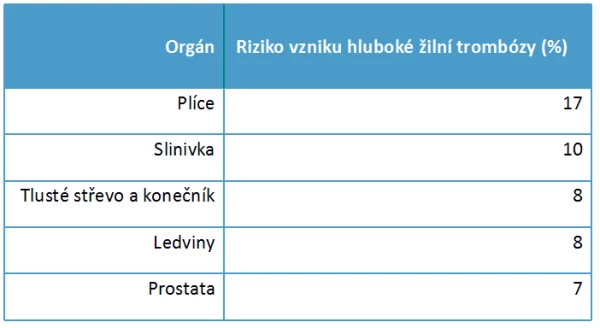
Nicméně, tromboembolizmus může předcházet diagnózu malignity [71-73]. V jedné studii bylo vyšetřeno 250 po sobě jdoucích pacientů se symptomatickou DVT a u 105 z nich byla následně zjištěna příčina nebo rizikový faktor pro rozvoj trombózy [71]. Zhoubný nádor byl identifikován při trombotické události v pěti (3,3 procenta) ze 153 pacientů bez jiných identifikovatelných rizikových faktorů.
Operační zákrok
Rizikem vzniku trombózy je i operace, zejména ortopedická, cévní, neurochirurgická a operace malignit [74 - 76].
Mezi další rizikové faktory v této skupině patří vyšší věk, předchozí žilní trombóza, trombofilie, anestézie, a čas imobilizace[74,76-81]. Bez profylaxe, je značně zvýšené riziko jak žilní trombózy, tak vzniku plicní embolie. Podle ACCP byly pacienti podstupující chirurgické zákroky rozděleni do následujících kategorií rizik (Tabulka 3) [82]:
- pacienti s nízkým rizikem, jsou ve věku do 40 let, nemají žádný z rizikových faktorů uvedených výše, budou vyžadovat celkovou anestezii na méně než 30 minut. Bez profylaxe je riziko proximální žilní trombózy menší než 1,0 procento, a nebezpečí ohrožení života plicní embolií je méně než 0,01 procenta.
- pacienti se středním rizikem, jsou ve věku nad 40 let, budou vyžadovat celkovou anestezii na více než 30 minut, a mají jeden nebo více z výše uvedených rizikových faktorů. Bez profylaxe, je riziko vzniku proximální žilní trombózy 2 - 10 procent, a riziko smrtelné plicní embolie je 0,1 - 0,7 procenta.
- u vysoce rizikových pacientů, ve věku nad 40 let, kteří musí podstoupit operaci pro maligní onemocnění nebo z ortopedické příčiny a operace trvající déle než 30 minut. Riziko proximální žilní trombózy je 10 - 20 procent a fatální plicní embolie 1 - 5 procent.
Tromboprofylaxe významně snižuje výskyt symptomatické DVT nebo plicní embolie v bezprostředním pooperačním období. Nicméně pokračuje riziko hluboké žilní trombózy po propuštění z nemocnice [83-86].
V následujících třech měsících se odhaduje riziko vzniku DVT na 2,2 procenta (95% CI: 1,4 – 3,0) a plicní embolie na 0,05 procenta (95% CI: 0,0-0,12) [87].
Trauma
Riziko trombózy se zvyšuje u všech závažných poranění [89 až 92]. Mechanizmy aktivace koagulačního systému po operaci nebo traumatu nejsou úplně známy, ale mohou zahrnovat snížený žilní průtok krve v dolních končetinách, zmenšenou fibrinolýzu, imobilizaci, uvolnění tkáňového faktoru a vyčerpání endogenních antikoagulačních faktorů, jako je antitrombin [93]. Lehká zranění jsou spojena se tří až pětinásobným nárůstem rizika DVT. U nosičů mutace faktoru V Leiden je toto riziko 50krát větší.
Orální a transdermální antikoncepce
Při správném používání se jedná o jednu z nejspolehlivějších a nejbezpečnějších reverzibilních způsobů antikoncepce.
Počínaje rokem 1995 se objevují epidemiologické studie, které prokazují vyšší riziko tromboembolické nemoci u kombinované perorální antikoncepce (CHC – combined hormonal contraception) obsahující gestoden a desogestrel (tzv. pilulky třetí generace), v porovnání s produkty obsahující levonorgestrel (tzv. pilulky druhé generace) [5] - [10 ]. Podobné zvýšené riziko bylo nedávno pozorovány u žen užívajících kombinovanou orální antikoncepci obsahující drospirenon (produkt tzv. čtvrté generace) [10] - [12].
Tato data byla potvrzena v posledním celoevropském přehodnocení rizika vzniku trombóz při užívání antikoncepce, kdy Farmakovigilační výbor pro posouzení rizik (PRAC) a následně i Výbor pro humánní léčivé přípravky (CHMP) Evropské agentury pro léčivé přípravky (EMA) v roce 2013 informoval, že roční incidence žilní tromboembolie je u přípravků s levonorgestrelem, norethisteronem a norgestimátem 5–7, u přípravků s etonogestrelem a norelgestrominem 6–12 a u přípravků s drospirenonem, gestodenem a desogestrelem 9–12 případů na 10 000 uživatelek CHC. Rovněž u cyproteron acetátu je podle přezkoumání EMA riziko VTE nízké a dobře známé a dosahuje úrovně HA obsahujících gestoden, desogestrel nebo drospirenon (tj. 9–12/10.000). Z důvodu minimalizace rizika doporučila EMA podávat tento přípravek pouze v léčbě akné související s androgenovou senzitivitou anebo hirsutismu, kde selhala topická léčba nebo systémová antibiotická léčba, a nekombinovat s jinými HA. Závěr tohoto přehodnocení potvrzuje přínos CHC v prevenci nechtěných těhotenství nad riziky a doporučil informovat ženy o riziku tromboembolie a jejích projevech s důrazem na individuální přístup ke každé pacientce.
Vzhledem k velkému rozšíření je perorální antikoncepce (OC) nejvýznamnější příčinou trombózy u mladých žen [108-110]. Riziko trombózy stoupá do čtyř měsíců od zahájení léčby a nebo při restartu po přestávce čtyř a více týdnů. Riziko se snižuje na předchozí úroveň do tří měsíců od ukončení. Zvýšené riziko VTE bylo také zjištěno i žen užívajících antikoncepční transdermální náplasti.
Ženy užívající kombinovanou orální antikoncepci jsou vystaveny zvýšenému riziku žilní tromboembolie [1], [2] a, v menší míře, arteriální tromboembolie [3], [4]. Na rozdíl od rizika arteriální tromboembolie, riziko žilní tromboembolie se liší podle typu progestagenu, které obsahují.
Klasifikace kombinované hormononální antikoncepce podle typu gestagenu

Přípravky, které obsahují levonorgestrel, norgestimát nebo norethisteron jsou spojeny s nejnižším rizikem VTE.
Estrogen obsažený v perorálních antikoncepčních prostředcích má schopnost aktivovat srážení krve. Nízkodávovaná perorální antikoncepce je spojena s nižším rizikem tromboembolie, než používání orální antikoncepce s vyšší hladinou estrogenu. Přesto, že užívání perorální antikoncepce není spojeno s detekovatelný hyperkoagulačním stavem u většiny žen, zvýšené riziko je kuřaček, u žen s hyperlipidémií či dyslipidémií, u ženy s cévními diabetickými změnami, u hyprtoniček a obézních.
U všech žen, které se rozhodnou pro hormonální antikoncepci, by měly být uváženy rizikové faktory pro tromboembolickou nemoc: obezita, vyšší věk, pozitivní rodinná anamnéza, dlouhodobá imobilizace, velký chirurgický zákrok v anamnéze, jakýkoliv chirurgický výkon na nohou a v pánvi, neurochirurgické operace, poúrazové stavy, a zdravotní stavy spojené s vyšším výskytem tromboembolické nemoci jako je rakovina, systémový lupus erytematodes, hemolyticko-uremický syndromu, chronické zánětlivé střevní onemocnění a srpkovitá anemie [xvii, xviii, xix ]. Lékaři i ženy by si měli být vědomi všech rizik a ihned věnovat pozornost varovným příznakům, které by mohly vést včasnému lékařskému zákroku.
V kontrolní skupině žen, které nepoužívají CHC a nejsou těhotné je incidence VTE asi 2 na 10 tisíc za rok.
Úroveň rizika u každé jednotlivé ženy záleží potom především na přítomnosti rizikových faktorů. U žen , které používají nízkodávkovanou CHC (<50 mikrogramů ethinylestradiolu) je výskyt VTE asi 6-12 na 10 tisíc za rok.
Je vhodné zmínit, že riziko VTE při používání nízkodávkované CHC je nižší, než během fyziologického těhotenství či v poporodním období. VTE může být fatální u 1-2% případů.
Kouření je významným rizikovým faktorem VTE a proto by ženy, které chtějí užívat CHC neměly kouřit. Ženám nad 35 let, které nadále kouří, by se měla důrazně doporučit jiná metoda antikoncepce.
Zvýšení frekvence nebo závažnosti migrény během používání CHC (které mohou být prodromem cerebrovaskulární příhody), může být důvodem k okamžitému vysazení.
Hormonální substituční terapie
Iniciativa o zdraví žen (Women's Health Initiative - WHI), se věnuje dlouhodobé strategii prevence srdečních onemocněních, rakoviny prsu a kolorekta a osteoporotických zlomenin u žen. Od roku 1993 shromáždila data o 161 808 ženách mezi 50-79 rokem a zhodnotila je v řadě randomizovaných studiích. Od konce roku 2005 byla tato studie prodloužena až na roky 2010-2015). Tato studie změnila přístup k prevenci a léčbě řady onemocněn v postmenopauze.
Meta-analýza WHI hodnotila také vztah mezi hormonální substituční terapií (HRT) a žilním trombembolizmem. Bylo zjištěno, že HRT způsobila přibližně dvojnásobný nárůst rizika VTE, který je největší v prvním roce léčby [xx, xxi,xxii,xxiii, xxiv].
Riziko pro VTE po užívání HRT dále stoupá u starších žen, stejně tak i u obézních, u žen s trombofilií (např. faktor V Leiden, mutace genu pro protrombin) nebo u žen s anamnézou tromboembolické příhody [xxv, xxvi, xxvii, xxviii, xxix, xxx].
Tamoxifen
Řada studií, včetně velkých Breast Cancer Prevence Trials, prokázala, že používání tamoxifenu je spojeno se zvýšenou mírou žilních trombóz a že má prokoagulační efekt, pokud je tamoxifen přidán k chemoterapii [122,123]. Všechny dostupné randomizované studie prokazují trend k vzniku více žilních příhod v rameni obsahujícím tamoxifen oproti rameni bez tamoxifenu.
Hluboká žilní trombóza v těhotenství (DVT)
Těhotenství je samo o sobě spojeno se zvýšeným rizikem rozvoje trombózy, která může být částečně v důsledku mechanické obstrukce žilního návratu útlakem zvětšenou dělohou, jakož i z hyperkoagulačního stavu spojeného s těhotenstvím. DVT je velmi závažnou komplikací, kdy je ohrožena nejen žena, ale i plod.
VTE se může projevit v průběhu těhotenství izolovaně na dolních končetinách jako hluboká žilní trombóza nebo může dojít k uvolnění sraženiny do plic a způsobit tak plicní embolii (PE) [xxxi, xxxii]. Podle literárních údajů je PE sedmou nejčastější příčinou úmrtí matky, zodpovědné za 9 procent z celkového počtu úmrtí matek [xxxiii, xxxiv].
Epidemiologie
Celková prevalence VTE v těhotenství je nízká. V Evropě byl v retrospektivní studii s více jak 72000 těhotnými prokázán výskyt DVT s frekvencí 7,1 na 10 tisíc porodů (95% CI 5 - 9) a výskyt PE byl 1,5 na 10 tisíc porodů.
Dvě studie ukazují, že výskyt VTE má v průběhu posledních tří desetiletí klesající trend, a to zejména díky snížení výskytu VTE v poporodním období [xxxv]. Důvody pro tuto změnu jsou nejasné, ale jsou nejčastěji vysvětlovány využíváním tromboprofylaxe v peripartálním období.
Rizikové faktory
Těhotenství samo o sobě zvyšuje riziko rozvoje VTE 4-50 krát ve srovnání s netěhotnými ženami [xxxvi, xxxvii, xxxviii, xxxix,xl, xli,xlii]. Zvýšené riziko VTE je ve všech fázích těhotenství, ale jednoznačně nejvyšší je v šestinedělí.
Rizikové faktory VTE lze dělit na pre - a postpartální:
Předporodní faktory
Většina studií udává rovnoměrné rozložení VTE napříč všemi trimestry těhotenství . Ovšem dvě velké retrospektivní studie uvedly většinu v prvním trimestru (40 procent před 15 týdnem) a potom až ve třetím trimestru (60 procent) [xliii, xliv].
K faktorům, zvyšujícím předporodní riziko VTE patří: [xlv]
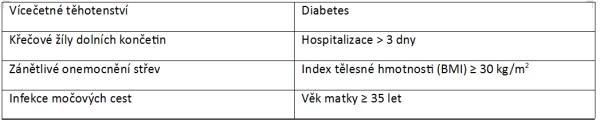
Poporodní faktory
VTE je dva až pětkrát častější po porodu, než před porodem, s tím že riziko je nejvyšší v prvních šesti týdnech.
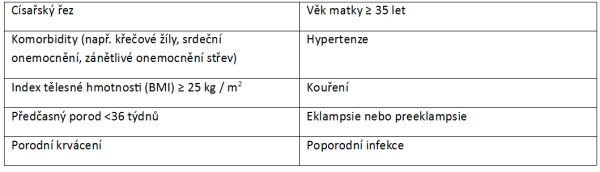
K faktorům, které zvyšují poporodní riziko, patří:
Anatomická lokalizace hluboké žilní trombózy
Mimo těhotenství postihuje DVT většinou obě dolní končetiny. Výskyt pánevní žilní trombózy se významně zvyšuje v průběhu těhotenství a šestinedělí.
V těhotenství postihuje DVT nejčastěji levou dolní končetinu (70-90 procent). V jedné studii bylo 60 těhotných žen s první epizodou VTE. U 58 z nich byla izolovaně postižena levá dolní končetina a jen ve dvou případech bylo bilaterální postižení. Za příčinu se pozvažuje zvýšený venózní tok v levé noze útlakem levé ilické žíly těhotnou dělohou
V těhotenství je také častější DVT pánevních žil než u běžné, netěhotné populace. Výskyt DVT v těhotenství některé studie uvádějí až ve 12 procentech ve srovnání s 1 procentem mimo těhotenství.
Diagnostika žilní trombózy v těhotenství:
V laboratorním obraze je u těhotných typicky zvýšená hladina koagulačních faktorů a inhibitorů fibrinolýzy. Vlastní trombogeneza je při fyziologickém těhotenství velmi pečlivě kontrolována aktivní inhibicí, která se udržuje celé těhotenství až do porodu. K většině tromboembolií proto dochází až po porodu.
Hlavním příznakem hluboké žilní trombózy je bolest a otok nejčastěji levé dolní končetiny, který může a nemusí být spojen s erytémem. Sonografie je zlatým standardem v diagnostice hluboké žilní trombózy spolu s vyšetřením D-dimerů. Dojde-li k plicní embolii, těhotná se stává náhle dušnou, má bolest na prsou a může dojít až k šokovému stavu. Při podezření na plicní embolii je hlavní diagnostickou metodou CT angiografie. Někdy pomůže i nález na EKG (P pulmonale a přetížení pravé komory) a rentgen plic.
Léčba TEN v těhotenství:
Protože perorálních antikoagulancia procházejí přes placentární bariéru a mohou zvýšit riziko krvácení u plodu, je v léčbě preferováno použití nízkomolekulárních heparinů (LMWH). U všech žen s prodělanou TEN v anamnéze je doporučována poporodní profylaxe LMWH po dobu celého šestinedělí. U žen s vyšším rizikem recidivy TEN podáváme LMWH i antepartálně a také u žen, které byly léčeny pro TEN před otěhotněním. Přihlíží se i k dalším rizikům – věku, přítomnosti varixů, obezitě apod. v celkovém hodnocení pro - a proti profylaxi v nejednoznačných indikacích. Profylaktickou therapii je nejlepší vést trombocentrech. U žen, které nikdy neprodělaly TEN a jsou nosičkami homozygotní mutace faktoru V Leiden nebo homozygotní mutace protrombinu se podává profylaktická dávka LMWH i antepartálně a poté celé šestinedělí. U ostatních trombofilních stavů, kdy žena neprodělala TEN v anamnéze, se doporučuje pouze předporodní klinické sledování a podání profylaktické poporodní dávky LMWH. U žen s opakovanými těhotenskými komplikacemi – opakované (více než 3) časné potraty do 10. týdne těhotenství je vhodné vyloučení antifosfolipidového syndromu a podání profylaktické dávky LMWH spolu s nízkou dávkou aspirinu (100mg/den).
Účinek léčby LMWH se laboratorně monitoruje pomocí hladiny inhibice FXa, kdy se odebere žilní krev za 4 hodiny po subkutánní aplikaci LMWH. Po profylaktické dávce má být anti-FXa 0,2-0,4 IU/ml, při terapeutických dávkách se má docílit hodnot 0,6-1,0 IU/ml.
Závěr
V chirurigických oborech se od počátku 90. let podařilo snížit incidenci pooperačních žilních trombóz zavedením heparinové profylaxe. Při vzniku žilní trombózy působí většinou několik příčin současně a jejich účinek se násobí. Rozhodování o tromboprofylaxi se řídí jak individuálními riziky, tak by měla být prováděna ve spolupráci se specializovanými trombotickými centry.
Seznam použitých zkratek
TEN - TromboEmbolická Nemoc (TEN)
VTE - žilní tromboembolizmus (Venous ThromboEmbolism)
DVT - hluboká žilní trombóza (Deep Venous Thromboembolism)
SVT - povrchová žilní trombóza (Superficial Venous Thrombosis)
LMWH - nízkomolekulární heparin (Low Molecular Weight Heparin)
OC - orální kontracepce (Oral Contraception)
CHC - kombinovaná perorální antikoncepce/kontracepce (Combined Hormonal Contraception)
RR - Relativní Riziko
WHI - Iniciativa o zdraví žen (Women's Health Initiative)
HRT - hormonální substituční terapie (Hormon Replacement Therapy)
- i Dickson BC. Venous thrombosis: on the history of Virchow's triad. Univ Toronto Med J 2004; 81 : 166.
- ii Bagot CN, Arya R. Virchow and his triad: a question of attribution. Br J Haematol 2008; 143 : 180.
- iii Chengelis DL, Bendick PJ, Glover JL, et al. Progression of superficial venous thrombosis to deep vein thrombosis. J Vasc Surg 1996; 24 : 745.
- iv de Moerloose P, Wutschert R, Heinzmann M, et al.Superficial vein thrombosis of lower limbs: influence of factor V Leiden, factor II G20210A and overweight. Thromb Haemost 1998; 80 : 239.
- v Martinelli I, Mannucci PM, De Stefano V, et al. Different risks of thrombosis in four coagulation defects associated with inherited thrombophilia: a study of 150 families. Blood 1998; 92 : 2353.
- vi Decousus H, Quéré I, Presles E, et al. Superficial venous thrombosis and venous thromboembolism: a large, prospective epidemiologic study. Ann Intern Med 2010; 152 : 218.
- vii Martinelli I, Cattaneo M, Taioli E, et al. Genetic risk factors for superficial vein thrombosis. Thromb Haemost 1999; 82 : 1215.
- viii Mateo J, Oliver A, Borrell M, et al. Laboratory evaluation and clinical characteristics of 2,132 consecutive unselected patients with venous thromboembolism--results of the Spanish Multicentric Study on Thrombophilia (EMET-Study). Thromb Haemost 1997; 77 : 444.
- ix Margaglione M, Brancaccio V, Giuliani N, et al. Increased risk for venous thrombosis in carriers of the prothrombin G-->A20210 gene variant. Ann Intern Med 1998; 129 : 89.
- x Crowther MA, Kelton JG. Congenital thrombophilic states associated with venous thrombosis: a qualitative overview and proposed classification system. Ann Intern Med 2003; 138 : 128.
- xi Dahlbäck B. Advances in understanding pathogenic mechanisms of thrombophilic disorders. Blood 2008;112 : 19.
- xii Prandoni P, Lensing AW, Cogo A, et al. The long-term clinical course of acute deep venous thrombosis. Ann Intern Med 1996; 125 : 1.
- xiii Samama MM. An epidemiologic study of risk factors for deep vein thrombosis in medical outpatients: the Sirius study. Arch Intern Med 2000; 160 : 3415.
- xiv Elting LS, Escalante CP, Cooksley C, et al. Outcomes and cost of deep venous thrombosis among patients with cancer. Arch Intern Med 2004; 164 : 1653.
- xv Khorana AA, Francis CW, Culakova E, et al. Thromboembolism in hospitalized neutropenic cancer patients. J Clin Oncol 2006; 24 : 484.
- xvi Stein PD, Beemath A, Meyers FA, et al. Pulmonary embolism as a cause of death in patients who died with cancer. Am J Med 2006; 119 : 163.
- xvii Annex III. Amendments to relevant sections of the summary of product. EMA website. Available:http://www.ema.europa.eu/docs/en_GB/document_library/Referrals_document/Combined_hormonal_contraceptives/European_Commission_final_decision/WC500160274.pdf Accessed 2014 Mar 14.
- xviii Ku GH, White RH, Chew HK, et al. Venous thromboembolism in patients with acute leukemia: incidence, risk factors, and effect on survival. Blood 2009; 113 : 3911.
- xix Gross CP, Galusha DH, Krumholz HM. The impact of venous thromboembolism on risk of death or hemorrhage in older cancer patients. J Gen Intern Med 2007; 22 : 321.
- xx Miller J, Chan BK, Nelson HD. Postmenopausal estrogen replacement and risk for venous thromboembolism: a systematic review and meta-analysis for the U.S. Preventive Services Task Force. Ann Intern Med 2002; 136 : 680.
- xxi Grodstein F, Stampfer MJ, Goldhaber SZ, et al. Prospective study of exogenous hormones and risk of pulmonary embolism in women. Lancet 1996; 348 : 983.
- xxii Pérez Gutthann S, García Rodríguez LA, Castellsague J, Duque Oliart A. Hormone replacement therapy and risk of venous thromboembolism: population based case-control study. BMJ 1997; 314 : 796.
- xxiii Hulley S, Furberg C, Barrett-Connor E, et al. Noncardiovascular disease outcomes during 6.8 years of hormone therapy: Heart and Estrogen/progestin Replacement Study follow-up (HERS II). JAMA 2002; 288 : 58.
- xxiv Hulley S, Furberg C, Barrett-Connor E, et al. Noncardiovascular disease outcomes during 6.8 years of hormone therapy: Heart and Estrogen/progestin Replacement Study follow-up (HERS II). JAMA 2002; 288 : 58. 116. Cushman M, Kuller LH, Prentice R, et al. Estrogen plus progestin and risk of venous thrombosis. JAMA 2004; 292 : 1573.
- xxv Cushman M, Kuller LH, Prentice R, et al. Estrogen plus progestin and risk of venous thrombosis. JAMA 2004; 292 : 1573.
- xxvi Glueck CJ, Wang P, Fontaine RN, et al. Effect of exogenous estrogen on atherothrombotic vascular disease risk related to the presence or absence of the factor V Leiden mutation (resistance to activated protein C). Am J Cardiol 1999; 84 : 549.
- xxvii Rosendaal FR, Vessey M, Rumley A, et al. Hormonal replacement therapy, prothrombotic mutations and the risk of venous thrombosis. Br J Haematol 2002; 116 : 851.
- xxviii Herrington DM, Vittinghoff E, Howard TD, et al. Factor V Leiden, hormone replacement therapy, and risk of venous thromboembolic events in women with coronary disease. Arterioscler Thromb Vasc Biol 2002; 22 : 1012.
- xxix Herrington DM, Vittinghoff E, Howard TD, et al. Factor V Leiden, hormone replacement therapy, and risk of venous thromboembolic events in women with coronary disease. Arterioscler Thromb Vasc Biol 2002; 22 : 1012.
- xxx Høibraaten E, Qvigstad E, Arnesen H, et al. Increased risk of recurrent venous thromboembolism during hormone replacement therapy--results of the randomized, double-blind, placebo-controlled estrogen in venous thromboembolism trial (EVTET). Thromb Haemost 2000; 84 : 961.
- xxxi Chung I, Lip GY. Virchow's triad revisited: blood constituents. Pathophysiol Haemost Thromb 2003; 33 : 449.
- xxxii Blann AD. How a damaged blood vessel wall contibutes to thrombosis and hypertenasion. Pathophysiol Haemost Thromb 2003; 33 : 445.
- xxxiii Chengelis DL, Bendick PJ, Glover JL, et al. Progression of superficial venous thrombosis to deep vein thrombosis. J Vasc Surg 1996; 24 : 745.
- xxxiv de Moerloose P, Wutschert R, Heinzmann M, et al. Superficial vein thrombosis of lower limbs: influence of factor V Leiden, factor II G20210A and overweight. Thromb Haemost 1998; 80 : 239.
- xxxv Bertina RM. Genetic approach to thrombophilia. Thromb Haemost 2001; 86 : 92.
- xxxvi Lijfering WM, Rosendaal FR, Cannegieter SC. Risk factors for venous thrombosis - current understanding from an epidemiological point of view. Br J Haematol 2010; 149 : 824.
- xxxvii Goldhaber SZ. Risk factors for venous thromboembolism. J Am Coll Cardiol 2010; 56 : 1.
- xxxviii Dickson BC. Venous thrombosis: on the history of Virchow's triad. Univ Toronto Med J 2004; 81 : 166.
- xxxix Bagot CN, Arya R. Virchow and his triad: a question of attribution. Br J Haematol 2008; 143 : 180.
- xl Bertina RM. Genetic approach to thrombophilia. Thromb Haemost 2001; 86 : 92.
- xli Spencer FA, Emery C, Lessard D, et al. The Worcester Venous Thromboembolism study: a population-based study of the clinical epidemiology of venous thromboembolism. J Gen Intern Med 2006; 21 : 722.
- xlii Lowe GD. Virchow's triad revisited: abnormal flow. Pathophysiol Haemost Thromb 2003; 33 : 455.
- xliii Makris M, Preston FE, Beauchamp NJ, et al. Co-inheritance of the 20210A allele of the prothrombin gene increases the risk of thrombosis in subjects with familial thrombophilia. Thromb Haemost 1997; 78 : 1426.
- xliv Emmerich J, Rosendaal FR, Cattaneo M, et al. Combined effect of factor V Leiden and prothrombin 20210A on the risk of venous thromboembolism--pooled analysis of 8 case-control studies including 2310 cases and 3204 controls. Study Group for Pooled-Analysis in Venous Thromboembolism. Thromb Haemost 2001; 86 : 809.
- xlv van Vlijmen EF, Brouwer JL, Veeger NJ, et al. Oral contraceptives and the absolute risk of venous thromboembolism in women with single or multiple thrombophilic defects: results from a retrospective family cohort study. Arch Intern Med 2007; 167 : 282.
Kurz je již bez kreditace, vhodný k edukaci
Byl pro Vás kurz přínosný? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



