-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Videa
- Podcasty
Nové podcasty
Reklama- Kariéra
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaNeuropatická bolest
Datum publikace: 2. 9. 2019
Úvod
Neuropatická bolest (NB) je definována jako bolest generovaná nervovým systémem. Přímé poškození periferních tkání, typické pro nocicepční typ bolesti, není podmínkou jejího vzniku. K hlavním charakteristikám NB patří poruchy čití, chronický průběh, spontánní nebo neškodným podnětem provokovaná bolest v distribuci odpovídající inervační oblasti postižené části nervového systému a malá účinnost klasických analgetik. Hranice mezi neuropatickou a nocicepční bolestí není ostrá, v řadě případů se obě složky kombinují, což podmiňuje velkou variabilitu klinických potíží. NB se klasicky dělí podle anatomických a etiologických hledisek a nověji pak podle předpokládaných patofyziologických mechanismů bolesti. Na konkrétním klinickém obrazu se obvykle podílí různé patofyziologické mechanismy bolesti, a jde tedy o bolesti smíšené. Moderní terapie se snaží o cílené potlačení symptomů NB na základě jejich obecné patofyziologie bez ohledu na jejich etiologii.
Terapie NB musí být komplexní. Prvním předpokladem je správná diagnostika onemocnění, které NB vyvolalo, a jeho cílená léčba. Základem symptomatické léčby NB jsou antikonvulziva, antidepresiva v kombinaci s vhodným analgetikem. Léčba je dle konkrétní situace doplňována léčbou lokální, fyziatrickou a podpůrnou psychoterapií. U rezistentních případů indikujeme invazivní techniky – nervové blokády nebo implantovanou neurostimulaci – ve specializovaných centrech.
Neuropatické bolesti jsou závažné z medicínského i socioekonomického hlediska. Jde o postižení omezující kvalitu života postižených a často vedoucí k invalidizaci.
Epidemiologie
Chronická bolest postihuje celosvětově velkou část populace a významně přispívá k morbiditě a snížení kvality života a představuje značnou socioekonomickou zátěž. Prevalence se podle různých údajů odhaduje na 10 až 46 % celosvětové populace, z toho jde u více než 5 % o bolest vysoké intenzity. Častěji jsou postiženy ženy a sociálně znevýhodněné skupiny obyvatel. Na celkové prevalenci chronické bolesti se významně podílí neuropatická bolest. Například ve Velké Británii se odhadovalo, že NB postihuje asi 1 % obyvatel, novější studie ale hovoří o podílu až 8 %. Tento nárůst se vysvětluje lepší diagnostikou při zpřesnění kritérií, ale i nárůstem výskytu při stárnutí populace a s tím spojeným vzestupem výskytu chronických chorob, především diabetu.
Statistické údaje o prevalenci NB v ČR nejsou známy, ale lze předpokládat, že situace je srovnatelná: incidence NB v populaci minimálně kolem 1 %. V ambulancích léčby bolesti představují pacienti s neuropatickou bolestí asi čtvrtinu klientely. Výskyt a závažnost neuropatických bolestí narůstají se zvyšujícím se věkem. Až 50 % neuropatických bolestí postihuje osoby starší než 70 let.
Neuropatická bolest je syndromem, který prokazuje, že došlo k postižení somatosenzorického systému. Vyskytuje se proto u široké škály onemocnění periferního i centrálního nervového systému.
Objevuje se u 5 % úrazů periferních nervů, je častou komplikací metabolických polyneuropatií, zejména diabetické polyneuropatie (až 50 % diabetiků starších 60 let). Bolestivá diabetická neuropatie postihuje asi 15 % pacientů. Z bolestivých kraniálních neuropatií je nejčastější neuralgie trigeminu s incidencí 5–8 případů na 100 000 obyvatel. Je častější u žen a ve věku kolem 70 let. K častým příčinám NB patří radikulární kompresivní syndromy s incidencí až 200 na 100 000 obyvatel a syndrom karpálního tunelu s incidencí 105–276 na 100 000 obyvatel.
NB provází rovněž neuroinfekce (30 % pacientů v manifestní fázi HIV infekce, neuroborrelióza, herpes zoster). Nejčastější z této skupiny je postherpetická neuralgie – 7–27 % pacientů 3 měsíce po proběhlém onemocnění. Roční incidence neuralgie se odhaduje na 11–40 případů na 100 000 obyvatel.
Centrální NB vzniká při onemocnění míchy, senzitivních drah kmene, podkorových oblastí (zejména thalamu, capsula interna) i mozkové kůry. Objevuje se jako pozdní následek ischemické CMP v oblasti bazálních ganglií asi u 8–11 % případů. NB trpí asi 30 % osob s roztroušenou sklerózou, pokud dojde ke vzniku plaků v průběhu senzitivní dráhy na míšní nebo podkorové úrovni. U syringomyelie je neuropatická bolest spíše pravidlem než výjimkou – vyskytuje se u 75 % nemocných.
Obr. 1: Senzitivní mapa člověka zpředu
Zobrazuje radikulární dermatomy, v druhé polovině inervační oblasti periferních nervů. Povšimněte si, že segmenty C5–Th1 nemají zastoupení na trupu, kde hranice probíhá mezi segmenty C4 a Th2!
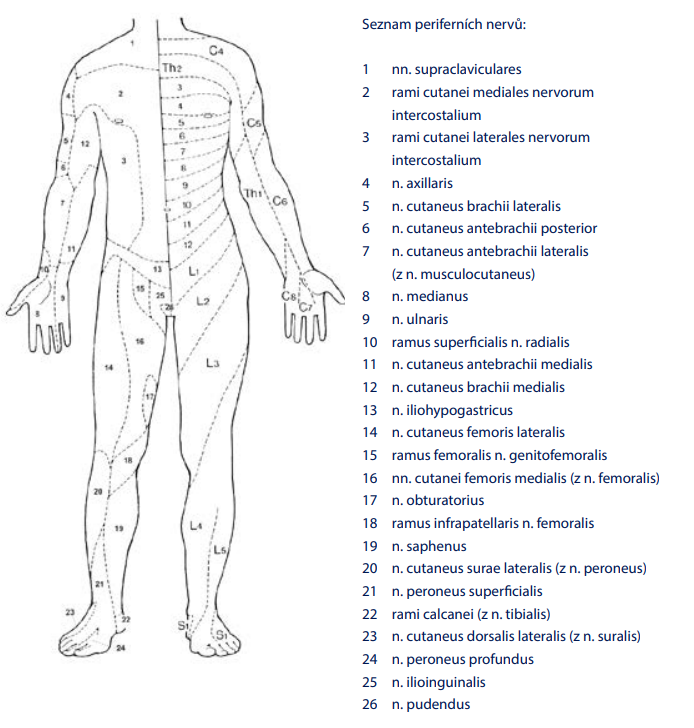
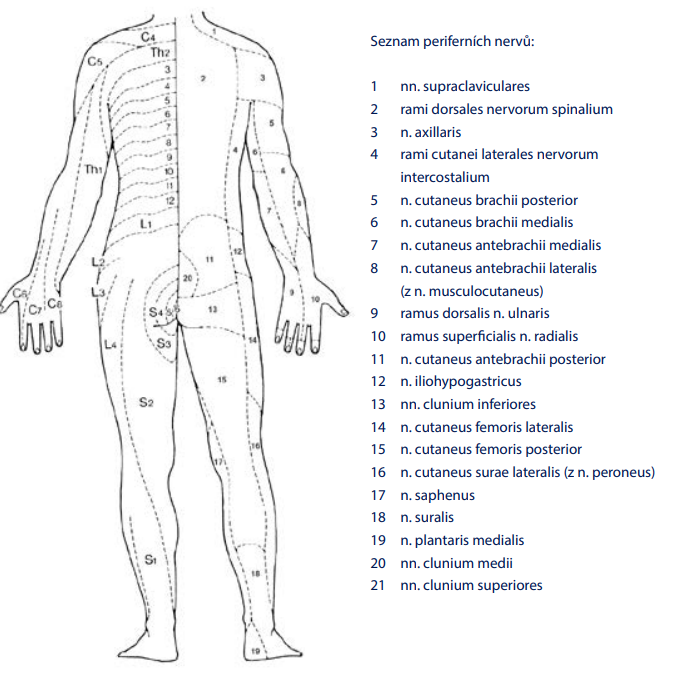
Obr. 2: Senzitivní mapa člověka zezadu
Zobrazuje radikulární dermatomy, v druhé polovině inervační oblasti periferních nervů.
Patofyziologie
NB je generována v periferních i centrálních částech somatosenzorického systému mnoha mechanismy. Podílí se na nich poškození i procesy regenerace na úrovni molekulární, tkáňové i celého organismu. Celkovým výsledkem je senzitizace nocicepčního systému na centrální i periferní úrovni, která je spolu se selháním sestupných drah modulujících bolest podkladem jeho hyperexcitability. Senzitizace představuje maladaptivní proces, jehož výsledkem je porušená filtrace bolestivých vstupů, pokles prahu bolesti a její tolerance a snadnější vznik potenciálů ve spinothalamické dráze. Podráždění vzniká v nervové dráze samotné, a to i bez přítomnosti poškození periferních tkání.
K senzitizaci dochází na všech etážích nervového systému. Nejvíce je tento proces prozkoumán na periferním nervu, dorzálním gangliu a v zadním míšním rohu, ze kterého vychází spinothalamická dráha. Současné výzkumy ale prokazují, že k podobným změnám dochází i na úrovni senzorického thalamu a do percepce bolesti zapojené kortikální sítě – „pain matrix“.
Podkladem periferní senzitizace je porucha funkce nebo poškození primárních aferentních vláken. Podílí se na ní několik procesů na více úrovních – zvýšení citlivosti periferních nociceptorů, zvýšená koncentrace sodíkových kanálů v membráně axonu (je podkladem zvýšené dráždivosti nervu), vznik ektopických vzruchů (spontánní vznik akčního potenciálu) a efapse (vznik akčního potenciálu přeskokem podráždění z taktilních na bolestivá vlákna). V některých případech hraje roli aberantní reinervace s přerůstáním sympatických synapsí na nocicepční vlákna periferního nervu (bolest udržovaná autonomní stimulací).
V míšních gangliích a zadních rozích míšních dochází při dlouhotrvající bolestivé stimulaci k nadměrnému uvolňování excitačních aminokyselin, zvýšené aktivitě NMDA receptorů, vápníkovému přetížení buňky, nadprodukci NO a kyslíkových radikálů. V důsledku těchto dějů dochází k remodelaci neuronálních okruhů zadního rohu a zvýšení aktivity projekčních neuronů dráhy bolesti. Při regeneraci navíc dochází k přerůstání zakončení z hlubších vrstev zadního rohu (taktilní čití) do oblasti bolestivé percepce. Klinickým projevem těchto změn je sekundární hyperalgezie, alodynie (vnímání nebolestivého podnětu bolestivě) a bolest chronicky udržovaná i po vyhasnutí nocicepčního dráždění.
Obdobné pochody probíhají i na vyšších etážích somatosenzorického systému, v mozkovém kmeni, thalamu a kůře. Uplatňuje se zde zkřížená aktivace sousedních neuronů, efaptická transmise vzruchové aktivity, denervační hypersenzitivita a redukce zpětnovazebné inhibice.
Průkaz senzitizace je důležitou součástí diagnostiky neuropatické bolesti. K symptomům prokazujícím etablovanou senzitizaci patří zejména alodynie, hyperalgezie, fenomén rozhořívání – zesilující se bolest při opakování podnětu – a aberantní zpracování senzorické stimulace – vjem přetrvává po ukončení stimulace, šíří se mimo stimulovanou oblast a má atypickou kvalitu.
Diagnostika
Podle doporučení Mezinárodní společnosti pro studium a léčbu bolesti klasifikujeme neuropatickou bolest do tří stupňů jistoty:
- možná neuropatická bolest,
- pravděpodobná neuropatická bolest,
- potvrzená neuropatická bolest.
Diagnóza probíhá ve dvou stupních: rozbor anamnézy a konfirmační vyšetření. Základním předpokladem pro úvahu o možné neuropatické bolesti je bolest projikovaná do anatomicky plauzibilní inervační oblasti (area nervina, kořenový dermatom, polyneuropatie, …). Druhým pilířem je zjištění, zda pacient trpí neurologickým onemocněním, které by mohlo podobnou symptomatiku způsobit. Ptáme se tedy, zda je pacient léčen pro diabetes mellitus, trpí vertebrogenním onemocněním, prodělal herpes zoster, cévní mozkovou příhodu apod. Zjišťujeme časovou souvislost. Proces senzitizace a vzniku neuropatické bolesti je obvykle subakutní v řádu několika týdnů, i když nelze zcela generalizovat. Časová souvislost je však obvykle zřetelná. Hlavním konfirmačním testem je neurologické vyšetření, které prokáže, zda jde skutečně o předpokládané postižení odpovídající topicky. Jeho nejdůležitější částí je vyšetření čití – jednoduchými prostředky si ověříme, že je skutečně přítomná polyneuropatická hypestezie apod. Další vyšetření mají potvrdit zvažovanou etiologii onemocnění (např. diabetes, herpetickou infekci, CMP). Kromě metod zaměřených na etiologii zde hraje zásadní roli elektrofyziologické vyšetření – elektromyografie, kondukční vyšetření periferních nervů, motorické a somatosenzorické evokované potenciály.
Možnou neuropatickou bolest diagnostikujeme, pokud jsou splněny oba anamnestické předpoklady, ale vyšetření je neprůkazné. Pravděpodobná neuropatická bolest je kategorie, při které potvrdíme poruchu senzitivity, ale další vyšetření zaměřená na etiologii jsou neprůkazná. Pokud se podaří prokázat i základní onemocnění, které je příčinou neuropatické bolesti, jde o potvrzenou neuropatickou bolest.
Klinické charakteristiky:
Přestože je neuropatická bolest obvykle popisována jako ostrá, šlehavá či elektrizující, nejsou žádné z těchto charakteristik pro NB patognomické. Klinická manifestace je mnohotvárná a prakticky vždy se kombinuje více projevů. Typická je kombinace trvalé tupé a hluboké bolesti, často s palčivou složkou, a povrchové ostré šlehavé bolesti, která se často provokuje senzorickou stimulací. Často používané charakteristiky při popisu neuropatické bolesti zahrnují pálivou bolest, bolestivý chlad, pocit elektrických výbojů, brnění, mravenčení, tupost a svědění.
Mnohdy je bolest paroxysmální nebo se trvalá a záchvatovitá bolest objevují společně. Intenzita bolesti je vysoká, obvykle 50 % rozsahu vizuální analogové škály a víc. Bolesti se zesilují pohybem postižené končetiny, zátěží, emočními vlivy nebo při interkurentním onemocnění. Pro diagnostiku jsou důležité i nebolestivé symptomy, které dělíme na pozitivní (parestezie – mravenčení, dysestezie – nepříjemné nebolestivé vjemy) a negativní – poruchy čití.
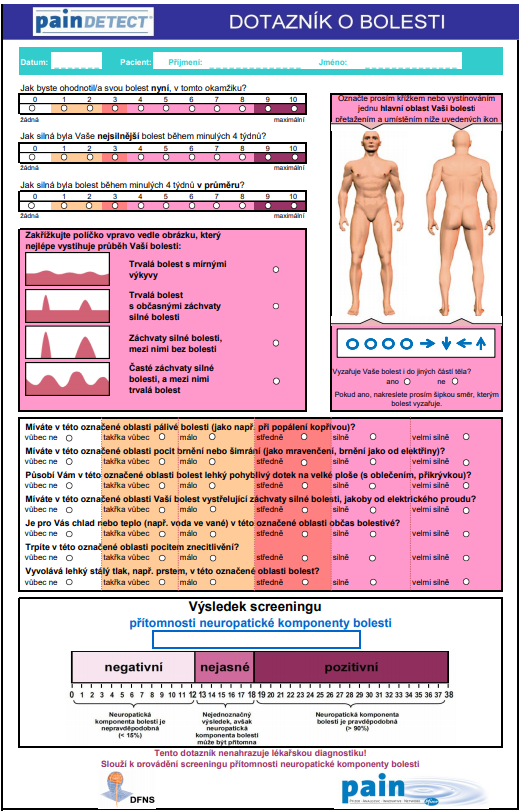
Vyšetření pacienta s neuropatickou bolestí zahajujeme anamnézou, při které se ptáme na charakter bolesti a přítomnost senzitivních poruch a jejich distribuci. Je výhodné použít validovaných dotazníků, které může pacient vyplnit ještě před vyšetřením. Nejvíce se u nás používá česká verze dotazníku PainDetect Německé společnosti pro studium neuropatické bolesti.
Obr. 3: Dotazník o bolesti – PainDetect (zdroj: https://www.pfizerpro.cz/sites/default/files/lyr-2017.02.007_pain_detect_cz.pdf)
Pro potvrzení diagnózy je nejdůležitější vyšetření čití, které je možné provést s použitím velmi jednoduchých prostředků. Pro základní vyšetření stačí špejle, vatová štětička, v ideálním případě kalibrovaná ladička Semmesův–Weinsteinův monofilament. Hodnotíme především distribuci poruchy čití, kterou můžeme zakreslit do somatosenzorické mapy se zobrazením radikulárních a nervových inervačních oblastí, viz obrázek. Vyšetřujeme základní modality – jemný dotek štětičkou, ostrý vjem třískou zlomené špejle nebo párátkem, kovovou část ladičky lze využít k vyšetření tepelného čití. Monofilamentem se vyšetřuje čití na bříšcích prstů na nohou. Pokud pacient cítí jen tři a méně z pěti doteků, je vysoké riziko neuropatie.
Z pomocných vyšetření má v praxi největší význam elektromyografie, která potvrzuje postižení silných myelinizovaných vláken periferních nervů. Neuropatie je často globální, tj. s postižením všech typů vláken probíhajících v nervu, ale je třeba vědět, že bolestivá složka neuropatie je vázána na tenká nervová vlákna, o jejichž funkci elektromyografie nevypovídá. Při selektivním postižení tenkých vláken je tedy EMG nález normální a neuropatickou bolest to nevylučuje. K dispozici je řada dalších vyšetřovacích možností k podrobnému mapování somatosenzorického systému (evokované potenciály, kvantitativní vyšetření čití, vyšetření autonomních funkcí, kožní biopsie, biopsie periferního nervu). Tato vyšetření jsou dostupná ve specializovaných centrech a jejich indikace je věcí specialisty.
Vyšetření zaměřená na určení etiologie neuropatické bolesti závisí na povaze onemocnění a zahrnují zobrazovací techniky, metabolické, sérologické, imunologické a další vyšetření potřebná v daném případě.
Přehled nejčastějších onemocnění, která způsobují neuropatickou bolest, je uveden přehledně v tabulce 1.
Tabulka 1: Častá onemocnění způsobující neuropatické bolesti podle anatomické lokalizace (pořadí podle četnosti)
Periferní nervy
Mícha
Mozek
diabetická polyneuropatie
roztroušená skleróza
cévní mozková příhoda
postherpetická neuralgie
traumatické léze
roztroušená skleróza
radikulární komprese
nádory
nádory, metastázy
neuralgie trigeminu
syringomyelie
syringomyelie
trauma
míšní ischemie
Parkinsonova nemoc
plexopatie
arachnoiditida
epilepsie
nádory
Léčba neuropatické bolesti
Obr. 4: Schéma léčby neuropatické bolesti
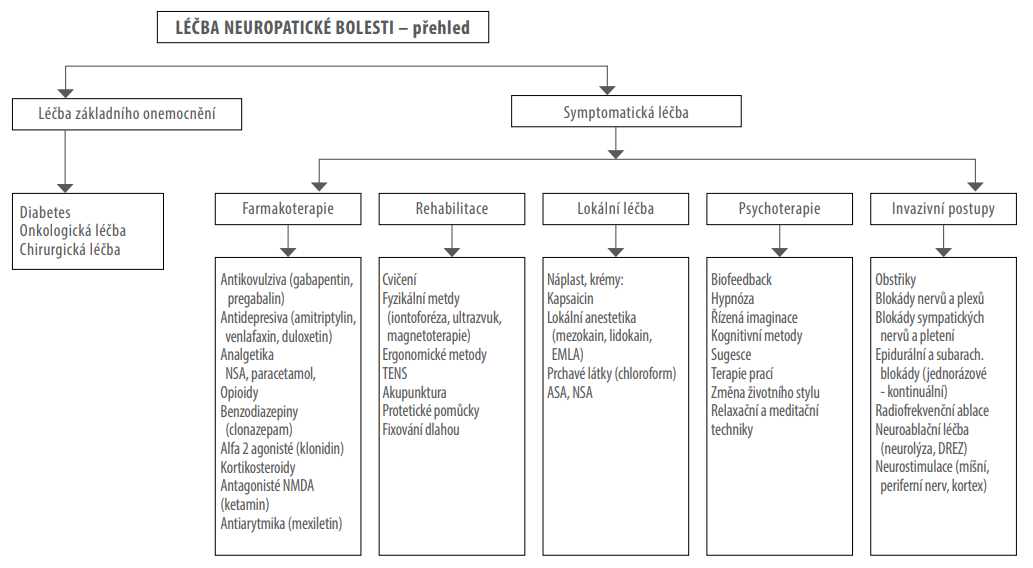
 Informace o léčbě jsou založeny na doporučených postupech českých a zahraničních odborných společností zabývajících se léčbou bolestí a monografií, které jsou uvedeny v doporučené literatuře.
Informace o léčbě jsou založeny na doporučených postupech českých a zahraničních odborných společností zabývajících se léčbou bolestí a monografií, které jsou uvedeny v doporučené literatuře.Léčba NB musí být komplexní a dlouhodobá, vyžaduje trpělivost lékaře i pacienta. Léčebný plán je vytvářen za aktivní spolupráce pacienta, který musí být realisticky informován o výhodách i rizicích léčby. Zejména je nutno upozornit na charakter nežádoucích účinků. Je důležité stanovení reálně dosažitelných cílů a kontrola jejich dosažení (kalendář bolesti, škály, dávky analgetik). Doporučujeme při každé návštěvě hodnotit a v dokumentaci zaznamenat efekt – pokles intenzity bolesti, např. numerickou škálou od 0 do 10 bodů – a toleranci – výskyt nežádoucích účinků a interakcí. Jako účinnou léčbu hodnotíme, pokud dojde k poklesu intenzity bolesti nejméně o dva body numerické škály. Ptáme se na spánek, náladu a celkovou spokojenost pacienta s léčbou. Tento postup zaručuje výrazně lepší adherenci k léčbě, která je obecně u dlouhodobé farmakoterapie nízká a během doby ještě klesá. Pacient musí zejména vědět, že cílem není úplná a rychlá eliminace bolestí, což se daří maximálně u čtvrtiny pacientů, ale redukce intenzity bolesti minimálně o třetinu a vypracování strategie, která povede ke zvýšení soběstačnosti a aktivity při běžných činnostech i např. rehabilitaci. Špatně informovaný pacient má tendenci rychle léky vysazovat pro „neúčinnost“, a léčba se tak stále vrací na začátek.
Terapie zahrnuje snahu o dobrou stabilizaci nebo eliminaci základního onemocnění, dále symptomatickou farmakoterapii, invazivní postupy (lokální blokády, neuromodulační a chirurgická léčba), psychoterapii a rehabilitaci.
Současným trendem v léčbě NB je léčba založená na ovlivnění jejích patofyziologických mechanismů. Základem farmakoterapie neuropatické bolesti jsou tzv. koanalgetika ze skupiny antikonvulziv (modulátory alfa2-delta podjednotky vápníkových kanálů, což vede ke snížení uvolňování excitačních aminokyselin na synapsi) a antidepresiv (zvýšení aktivity sestupných bolest modulujících drah). Oba přístupy se kombinují s analgetiky a invazivní a rehabilitační léčbou.
Výběr vhodného léku musí kromě bolesti zohledňovat i další faktory, především poruchy spánku a závažnost depresivity a úzkostí. Poruchy spánku a afektivity jsou u chronických bolestí v nějaké formě přítomny prakticky vždy a je třeba po nich cíleně pátrat. Vzhledem k riziku interakcí musíme brát v úvahu i komorbidity a další chronickou medikaci, kterou pacient užívá. Toto je důležité zvláště u starších osob. S nástupem farmakogenetiky a personalizované medicíny bude léčba určována i individuálním profilem polymorfismů cytochromu P450 a dalších geneticky určených faktorů. Tyto trendy se v praxi začínají uplatňovat již nyní a v krátké době jejich význam nepochybně poroste.
Dávkování a přehled hlavních vlastností léčiv používaných k léčbě neuropatických bolestí jsou uvedeny v tabulce č. 2.
Léky první volby zahrnují farmaka s nejvyšším účinkem nebo nejpříznivějším poměrem mezi účinkem a snášenlivostí. Jejich efektivita je prověřena dvojitě zaslepenými studiemi s dostatečným počtem pacientů. Patří sem tricyklická antidepresiva, antidepresiva inhibující zpětné vstřebávání serotoninu a noradrenalinu a antikonvulziva působící na vápníkový kanál – gabapentin a pregabalin. Tricyklická antidepresiva patří k nejstarším a stále nejúčinnějším lékům na neuropatickou bolest. Prototypem je amitriptylin, ale jeho efektivita se podstatně neliší od dalších tricyklik (nortriptylin, imipramin, klomipramin, dosulepin). Jejich působení je neselektivní, inhibují zpětné vstřebávání serotoninu a noradrenalinu, ale působí i na sodíkových kanálech, beta2-adrenergních a opioidních receptorech, mají výrazné anticholinergní a antihistaminové účinky. Ovlivnění celého spektra receptorů je zřejmě důvodem analgetické efektivity, ale zároveň příčinou četných nežádoucích účinků. Z nich je nejzávažnější prodloužení QT intervalu a tím zvýšené riziko kardiálních arytmií. U kardiaků jsou kontraindikována a u osob vyššího věku před jejich nasazením vždy indikujeme EKG. K dalším často uváděným problémům patří ortostatická hypotenze, centrální útlum, anticholinergní příznaky – obstipace, močová retence. Používáme nejnižší účinnou dávku, obvykle podávanou na noc, nepřekračujeme ekvivalent 75 mg amitriptylinu denně.
Venlafaxin a duloxetin patří do skupiny antidepresiv inhibujících zpětné vstřebávání serotoninu a noradrenalinu. Jejich účinnost je srovnatelná s tricyklickými antidepresivy, snášenlivost je ale podstatně lepší. Vzhledem ke zvýšení hladiny katecholaminů může docházet ke zvyšování krevního tlaku, který je nutno sledovat. U pacientů s nedostatečně léčenou hypertenzí nejsou tyto léky vhodné. Duloxetin je lékem první volby hlavně v případech bolestivé formy diabetické polyneuropatie. Častým problémem je nauzea nebo útlum, zahajujeme dávkou 30 mg, po týdnu zvyšujeme na 60 mg. Při renální insuficienci podáváme redukovanou dávku. Venlafaxin podáváme ve formě s prodlouženým uvolňováním, obvykle jednou denně, zahajujeme 75 mg denně, lze zvýšit na 150 mg denně. Hlavním nežádoucím účinkem je útlum nebo nauzea.
Antikonvulziva ze skupiny modulátorů alfa2-delta podjednotky vápníkových kanálů, gabapentin a pregabalin, mají sice vyšší číslo number needed to treat, ale podstatně menší počet nežádoucích účinků, lineární farmakokinetiku, nízké riziko lékových interakcí a rychlý nástup účinku. Jejich účinek se nesnižuje ani při dlouhodobé aplikaci. Nežádoucí účinky zahrnují zejména centrální útlum, ospalost, únavnost a pocity opilosti. Méně často se objevují periferní otoky, závratě a bolesti hlavy. Vzácnější jsou recidivující infekce, které ale nutí k vysazení léčby. Tyto léky patří dnes k nejčastěji používaným při léčbě neuropatické bolesti. Gabapentin podáváme třikrát denně, pregabalin dvakrát denně, jejich účinnost je srovnatelná, preparáty jsou zaměnitelné, tolerance individuální, při nesnášenlivosti gabapentinu lze zkoušet pregabalin i naopak.
Prostředky druhé volby nasazujeme při nedostatečném terapeutickém efektu léčby první linie (pokles intenzity bolesti o méně než 30 % škály). Prvním opatřením je záměna léků první volby (pacient léčený duloxetinem bude převeden na pregabalin a opačně).
K hlavním lékům druhé volby patří slabý opioid tramadol, výhodná je fixní kombinace s paracetamolem. Podává se ve čtyřhodinových intervalech, v případě preparátů s prodlouženým uvolňováním maximálně dvakrát denně. Maximální dávka je 400 mg denně. Nejčastějšími problémy jsou nauzea, útlum a vertigo. Pro riziko serotoninového syndromu je nutné kombinace s antidepresivy indikovat opatrně a stav pacienta kontrolovat. Riziko vzniku závislosti existuje i u tramadolu, přestože nižší než u silných opioidů.
Baklofen je myorelaxans působící jako agonista míšních GABA receptorů podtypu B. Uplatňuje se jako koanalgetikum druhé volby, zejména u neuralgie trigeminu. Podává se obvykle třikrát denně, počáteční dávka 15 mg se pomalu zvyšuje. Nepodáváme více než 60 mg denně. Je kontraindikován u epilepsie. Hlavním nežádoucím efektem je centrální útlum nebo nauzea či závratě.
Silné opioidy mají sice prokázaný efekt i u neuropatických bolestí, zvláště depotní formy morfinu a oxykodonu. Vzhledem k riziku vzniku závislosti patří ale jejich indikace do rukou specialistů. Ve specializovaných centrech je možné použít léčbu třetí volby a léčebné možnosti jsou rozšířeny o invazivní postupy uvedené v následující části.
V případě periferní lokalizované bolesti doplňujeme léčbu lokálními prostředky – náplastmi s 5% lidokainem nebo 8% kapsaicinem. Lidokainové náplasti se aplikují na 12 hodin na bolestivou plochu, maximální jednotlivá dávka jsou tři náplasti najednou. Kapsaicinovou náplast je možné aplikovat pouze po předchozí lokální anestezii na bolestivou plochu na 30 až 60 minut. Analgetický efekt trvá až tři měsíce a aplikaci lze opakovat. Systémové vstřebávání je minimální. K lokálním metodám léčby neuropatické bolesti patří i subkutánní aplikace botulotoxinu A. Účinnost tohoto postupu byla prokázána studiemi z poslední doby. Pro svou bolestivost se opět provádí v lokální anestezii u specialisty na léčbu bolesti.
Z postupů, které se v zaslepených studiích neosvědčily, je možné uvést mexiletin, klonidin a NMDA antagonisty. Antidepresiva třídy SSRI (selective serotonine re-uptake inhibitors) neprokázala koanalgetický efekt, i když studie z poslední doby ukázaly efekt při použití vyššího dávkování. Podle platných doporučení ale nejsou zatím k léčbě bolesti indikována, stejně jako antikonvulziva jiná než působící na alfa2-delta podjednotce vápníkového kanálu. V tomto smyslu se mění postavení karbamazepinu, který podle poslední revize doporučení Evropské neurologické společnosti není k léčbě neuropatické bolesti indikován, přestože je tak dlouhodobě používán. V každém případě se tak přesouvá do třetí linie.
Přehled léčebných možností u nejčastějších neuropatických bolestí je uveden v tabulce 2.
Tabulka 2: Přehled farmak užívaných v léčbě neuropatických bolestí
Preparát
Mechanismus účinku
NNT pro 50% pokles intenzity bolesti – průměr
Nežádoucí účinky
Kontraindikace
antidepresiva: amitriptylin, nortriptylin, imipramin, klomipramin, dosulepin
inhibice zpětného vstřebávání monoaminů
blokáda sodíkového kanálu
3,6
somnolence, prodloužení QT intervalu, anticholinergní efekt, váhový přírůstek
kardiální onemocnění, hyperplazie prostaty, glaukom, epilepsie
antidepresiva: venlafaxin, duloxetin
inhibice zpětného vstřebávání serotoninu a noradrenalinu
6,4
nauzea, obstipace, dekompenzace hypertenze u venlafaxinu
jaterní a renální poruchy, hypertenze, kardiální onemocnění
antikonvulziva: gabapentin, pregabalin
modulátory alfa2-delta podjednotky vápníkových kanálů
6,3 gabapentin
7,7 pregabalin
somnolence, nauzea, periferní otoky, váhový přírůstek
renální insuficience
tramadol
Duální efekt: agonista µ-opioidních receptorů,
inhibice zpětného vstřebávání monoaminů
4,7
nauzea, zvracení, obstipace, somnolence
opatrně kombinovat s antidepresivy, riziko závislosti
silné opioidy: oxykodon, morfin
agonisté µ-opioidních receptorů
4,3
nauzea, zvracení, obstipace, somnolence
závislost, riziko suicidia
baklofen
agonista GABAB receptoru
?
somnolence, závratě, bolesti hlavy
epilepsie
karbamazepin
blokáda sodíkových kanálů
1,4–2,8 u neuralgie trigeminu
somnolence, nauzea, toxoalergický exantém, hyponatremie, interakce – induktor jaterních enzymů
atrioventrikulární blokáda, jaterní insuficience, útlum kostní dřeně
lokální léčba: lidokain
blokáda sodíkových kanálů
?
lokální iritace
lokální afekce
kapsaicin
destrukce vaniloidních receptorů typu 1
10,6
lokální bolest a iritace
lokální afekce
botulotoxin A
blokáda acetylcholinových receptorů a neuromuskulárního přenosu
1,9
lokální bolest
lokální afekce
NNT (number needed to treat) – počet pacientů které je nutno léčit, abychom dosáhli úspěchu
Tabulka č. 3: Přehled léčby u běžných příčin neuropatické bolesti
Bolestivý syndrom
Lék 1. volby
Lék 2. volby
Doloženo randomizovanými studiemi (RCT)
bolestivé polyneuropatie
TCA, gabapentin, pregabalin, duloxetin, venlafaxin
SNRI, tramadol, opioidy
úroveň důkazu A
postherpetická neuralgie
gabapentin, pregabalin, TCA
opioidy, valproát, kapsaicin
úroveň důkazu A
primární neuralgie trigeminu
karbamazepin
baklofen, lamotrigin
úroveň důkazu A
centrální neuropatická bolest
TCA, gabapentin, pregabalin
lamotrigin, opioidy
úroveň důkazu B
TCA – tricyklická antidepresiva, SNRI – serotonin-noradrenalin re-uptake inhibitor, RCT – randomised controlled study
Úroveň důkazu A – efekt prokázán nejméně jednou prospektivní RCT studií s dostatečným počtem pacientů nebo dvěma prospektivními kohortovými studiemi případů a kontrol
Úroveň důkazu B – nejméně jedna přesvědčivá prospektivní kontrolovaná studie
Intervenční léčba periferní neuropatické bolesti
Invazivní postupy je možné indikovat v případech, kdy selhala standardní léčba neuropatické bolesti, byly vyčerpány farmakologické terapeutické metody, včetně použití opioidů a lokální terapie. Pacienty k indikaci intervenčních metod odesíláme na specializované pracoviště léčby bolesti.
Nejčastěji používanou invazivní léčbu představují nervové blokády a perineurální infiltrace lokálními anestetiky s kortikosteroidy, méně častou neurolytické postupy. Neurolytické postupy se nejčastěji používají na interkostální nervy při použití vysoce koncentrovaného alkoholu (96% koncentrace). U interkostálních nervů nehrozí motorické postižení nervových struktur, nicméně je potřeba uvážit i možnost iritačního postižení nervu s následným zhoršením bolestivého stavu. Častěji se proto používají obstřiky s lokálním anestetikem a kortikosteroidem, které je možné aplikovat současně i ve více etážích k jednotlivým interkostálním nervům.
Nervové blokády periferních nervů a hlavových nervů se provádějí pod sonografickou navigací, správná lokalizace se ověřuje neurostimulačním přístrojem. Při správném provedení zajištěném specializovaným vybavením jde o velmi bezpečné a efektivní metody léčby bolesti. Vzhledem k nutnosti uvedeného vybavení se tyto postupy provádějí na specializovaných pracovištích, která mají dostatečné klinické zkušenosti s invazivní léčbou bolesti.
Při postižení periferních nervů se provádí periferní nervové bloky jednorázové nebo po zavedení perineurálního katétru s opakovanou aplikací léčebné směsi. Chronické bolesti dolní části bederní páteře je možné ovlivnit sérií kaudálních blokád. Při lokalizaci bolesti na úrovni vyšších bederních nebo hrudních segmentů se provádějí epidurální blokády, obvykle s opakovanou aplikací po zavedení katétru do epidurálního prostoru.
Další šetrnou invazivní metodu představuje pulzní radiofrekvenční termoléze, která pracuje s teplotou na hrotu jehly do 42 stupňů. Tento postup může šetrně ovlivnit vedení v nervové struktuře včetně vedení bolesti bez známek postižení periferního nervu.
Nejvíce sofistikovanou invazivní léčbu v současnosti představuje neuromodulační terapie implantovaným systémem. Provádí se v neuromodulačních centrech, obvykle ve fakultních nemocnicích. Nejčastější z těchto metod je míšní stimulace. Pokud se jedná o postižení jednotlivého periferního nervu, lze aplikovat periferní nervovou stimulaci. U míšní stimulace se stimulační elektroda zavádí do epidurálního prostoru páteře, který odpovídá lokalizaci postižení. Během zavedení elektrody v lokální anestezii testujeme analgetický efekt elektrickou stimulací, která má u pacienta místo jeho chronické bolesti vyvolat pocity příjemného brnění. Po zkušebním období (asi týden) je pacientovi podkožně implantován generátor pulzů a pacient si sám ovládá analgetickou stimulaci telemetrickým ovladačem v domácích podmínkách.
Periferní nervová stimulace se provádí zavedením elektrody přímo k postiženému nervu při použití navigačních přístrojů (většinou se využívá sonografie, jehlová stimulace a rtg.), navigace je nezbytná vzhledem k tomu, že je potřeba elektrodu umístit do bezprostřední blízkosti nervu.
Pacient, který je indikován k neurostimulačním metodám, musí absolvovat podrobná a komplexní předoperační vyšetření odborníky multidisciplinárního týmu, a to i vzhledem k tomu, že se jedná o velmi nákladnou metodu a zavedení techniky je prakticky doživotní a představuje pro pacienta určitá režimová opatření.
Závěrečná doporučení pro praxi:
- Prvním krokem je správná diagnóza syndromu neuropatické bolesti včetně stanovení jeho etiologie.
- Zahájíme kauzální léčbu zaměřenou na příčinu neuropatické bolesti (pokud je možná).
- Symptomatickou farmakoterapii neuropatické bolesti zahajujeme v případě, že neuropatická bolest je střední a vyšší intenzity a způsobuje pacientovi utrpení.
- Lék první volby vybíráme s přihlédnutím k etiologii a komorbiditám.
- Pravidelně hodnotíme efekt léčby podle intenzity bolestí, nejlépe s použitím některé z validovaných škál, a hodnotíme výskyt nežádoucích účinků.
- A) Pokud je léčba účinná, neměníme ji. Pravidelně přehodnocujeme nutnost pokračovat v léčbě, v případě příznivého vývoje se snažíme v perspektivě několika měsíců léčbu postupně vysazovat.
- B) Při částečném efektu zvyšujeme dávku nebo přidáme další lék první nebo další volby.
- C) Pokud je léčba neúčinná, vyměníme lék za jiný ze skupiny první volby.
- Při neúčinnosti farmakologické léčby i s použitím více preparátů první a druhé volby pacienta odesíláme do specializované ambulance nebo centra léčby bolesti k indikaci nefarmakologických a invazivních metod léčby.
- Opavský J. Bolest v ambulantní praxi. Maxdorf; 2011.
- Slíva J., Kozák J., Černý R. Farmakoterapie neuropatické bolesti. Maxdorf; 2011.
- Bednařík J., Ambler Z., Opavský J., Keller O., Rokyta R. Klinický standard pro farmakoterapii neuropatické bolesti. Česká a Slovenská neurologie a neurochirurgie; 2017, s. 1–9.
- Treede R. D., Jensen T. S., Campbell J. N., Cruccu G., Dostrovsky J. O., Griffin J. W., Hansson P., Hughes R., Nurmikko T., Serra J. Neuropathic pain: Redefinition and a grading system for clinical and research purposes. Neurology. 2008 Apr; 70 : 1630–1635.
- Attal N., Cruccu G., Baron R., Haanpää M., Hansson P., Jensen T. S., Nurmikko European Federation of Neurological Societies. EFNS guidelines on the pharmacological treatment of neuropathic pain: 2010 revision. European Journal of Neurology. 2010 Sep; 17 : 1113–e1188.
- Attal N. Pharmacological treatments of neuropathic pain: The latest recommendations. Rev. Neurol. (Paris). 2019 Feb; 175 : 46–50.
- Centre for Clinical Practice at NICE (UK). Neuropathic Pain: The Pharmacological Management of Neuropathic Pain in Adults in Non-specialist Settings. London: National Institute for Health and Care Excellence, (UK); 2013 Nov; 1–33.
Kurz je již bez kreditace, vhodný k edukaci
Byl pro Vás kurz přínosný? Rádi byste se k němu vyjádřili? Napište nám − Vaše názory a postřehy nás zajímají. Zveřejňovat je nebudeme, ale rádi Vám na ně odpovíme.
Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



